Факторы риска развития
- Возраст
- Постменопаузальный период у женщин
- Поведенческие факторы: малоподвижный образ жизни и преобладание углеводной диеты
- Социально-экономический статус
На сегодняшний день мнения ученых о патофизиологии МС разделились на два лагеря. Одни считают, что в основе развития МС лежит ИР, по мнению других — эндотелиальная дисфункция, провоцирующая развитие как ИР, так и МС.
«Золотым стандартом» для определения инсулинорезистентности служит эугликемический гиперинсулинемический «клэмп»-тест как способ прямой оценки чувствительности к инсулину. Однако эта процедура стоит очень дорого, поэтому во многих стационарах провести ее практически невозможно. Для практических целей чаще используют непрямые методы — внутривенный и пероральный тест на толерантность к глюкозе.
Показатель инсулинорезистентности (ПИР) расчитывается по формуле M.R.Taskinen [1993]:
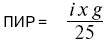
где i — уровень инсулина в крови натощак (мкЕД/мл), g — уровень глюкозы в крови натощак (ммоль/л).
Ожирение
Ожирение, по признанию ВОЗ, рассматривают как неинфекционную эпидемию настоящего времени в связи с его широким распространением среди населения, высоким риском развития ССЗ, ранней инвалидизацией больных и преждевременной смертностью.
По данным ВОЗ, около 30% жителей планеты страдают избыточным весом. Численность людей, страдающих ожирением, прогрессивно увеличивается каждые 10 лет на 10%.
Первенство в распространенности ожирения и избыточной массы тела среди стран держит Северная Америка: у половины населения США индекс массы тела (ИМТ) превышает 25. На втором месте — Великобритания, а на третьем — Россия, где более 30% трудоспособного населения страдает избыточной массой тела и ожирением.
Ожирение — это многофакторное хроническое рецидивирующее заболевание, характеризующееся избыточным содержанием жировой ткани в организме.
Жировые отложения располагаются:
- в подкожно-жировой клетчатке (подкожный жир);
- вокруг внутренних органов (висцеральный жир).
Абдоминальное ожирение — это избыточное расположение жира в подкожно-жировой клетчатке в области живота и висцерального жира в брюшной полости (абдоминальные жировые отложения).
Целый ряд исследований доказал, что сочетание именно абдоминального ожирения с повышением уровня триглицеридов приводит к развитию ИР.
IDF приняла пороговые значения ОТ для определения абдоминального ожирения: у мужчин — 94 см, у женщин — 80 см.
Таблица 1. Индекс массы тела
|
Масса тела |
Индекс |
Риск заболеваний |
|
Дефицит |
< 18,5 |
Низкий |
|
Нормальная |
18,5–24,9 |
Обычный |
|
Избыточная |
25–29,9 |
Повышенный |
|
Ожирение 1 ст. / болезнь |
30–34,9 |
Высокий риск |
|
Ожирение 2 ст. / болезнь |
35,0–39,9 |
Очень высокий |
|
Ожирение 3 ст. / болезнь |
> 40 |
Чрезвычайно высокий |
Таблица 2. Факторы, влияющие на ожирение
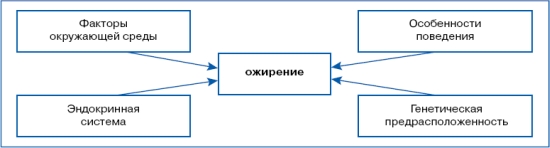
Факторы окружающей среды
Ожирение чаще встречается у населения крупных городов, чем у сельских жителей, у людей, занимающихся умственным, а не физическим трудом. Ожирение тем вероятней, чем ниже уровень образования (люди с невысоким уровнем образования менее склонны к самоограничению).
Поведение
Большое внимание уделяется изучению диеты — диетанамнезу.
Негативные факторы здесь — это нарушение режима питания, редкие приемы пищи, обильная еда в вечерние часы, сниженная физическая активность.
Генетическая предрасположенность и эндокринные нарушения
- Генетически обусловленный феномен, не позволяющий организму расходовать избыточные калории в виде тепла.
- Переедание в детском возрасте, формирующее функционально-морфологическую основу для реализации генетического феномена и развития ожирения.
- Неправильные привычки питания, повышение основного обмена, формирование порочных эндокринных реакций организма.
Согласно современным представлениям, ключевым механизмом ожирения являются конкретные нарушения гормональной связи между жировой тканью и гипоталамусом, раскрытые в середине 1990 г.
Именно из-за этих нарушений меняется пищевое поведение больного, его психология и тенденция к выбору определенного образа жизни.
Долгое время считалось, что ГИ способствует накоплению абдоминального жира и что именно ГИ есть пусковой фактор МС. Исходили из того, что абдоминальное ожирение является следствием снижения активности липолитических процессов. Гормоночувствительная липаза — основной фермент, контролирующий скорость липолиза в жировой ткани. Ее активизация происходит под влиянием катехоламинов посредством цАМФ — зависимого фосфорилирования, тогда как инсулин, повышая гидролиз цАМФ, ингибирует липолиз и повышает липогенез.
Однако на сегодняшний день существуют достаточно убедительные доказательства того, что ожирение не вызывается ИР.
Исследования резких изменений веса показали, что его экспериментальный набор приводит к повышению концентрации сывороточного инсулина, а потеря веса — к падению этой концентрации. Более того, уменьшение ИР в ответ на потерю веса было непосредственно продемонстрировано при использовании техники эугликемического гиперинсулинемического клампирования.
Было постулировано, что ИР развивается как защита от непрерывного несдержанного набора веса.
С этим согласуются данные восьмилетнего наблюдения SAN ANTONIOHEART STUDY, которые показывают, что у пациентов с ожирением, в отличие от худых, более высокие уровни инсулина являются предиктором скорее потери веса, чем его набора.
При этом интересно отметить, что на настоящий момент нет убедительных данных, свидетельствующих о том, что гиперинсулинемия способна увеличить риск развития ССЗ.
В развитии ожирения, МС, по-видимому, ведущую роль играют средовые и генетические факторы, приводящие к нарушению баланса потребления и метаболизма жиров. Продуктами секреции адипоцитов являются эстрогены, ангиотензиноген, простагландины, TNF, IL-6, лептин, инсулиноподобный фактор роста и связывающие белки, ингибитор активатора плазминогена I. В этом перечне следует выделить лептин — гормон, осуществляющий информационную связь между гипоталамусом и белой жировой тканью, интегрированный в систему обратной связи с гипоталамическими нейропептидами (в первую очередь, с нейропептидом Y 75). К числу регуляторов центра голода и насыщения относятся инсулин, холецистокинин, норадреналин и серотонин.
* * *
Открытие Y. Zhanq и соавторами (1994) гормона лептина, продуцируемого белой жировой тканью, стало значимым шагом в изучении ожирения.
До недавнего времени адипоциты считались «пассивными» клетками, в которых накапливается избыток энергии в виде триглицеридов. При этом диаметр клетки может увеличиться в 20 раз, а около 90% ее объема занимают отложения жира, которые смещают ядро и цитоплазму на периферию клетки.
Однако в настоящее время получены данные, которые убедительно свидетельствуют о том, что адипоциты являются активными клетками, секретирующими различные гормоны, факторы роста и цитокины.
Одним из основных гормонов жировой ткани считают лептин. Общее количество лептина в организме пропорционально массе жировой ткани и физиологически выше у женщин, нежели у мужчин.
Выработка лептина в адипоцитах стимулируется инсулином и, в меньшей степени, глюкокортикоидами и зависит от размеров жировых клеток.
Лептин проникает в гипоталамус и избирательно рецептируется вентро-медиальными ядрами. Он вызывает насыщение и продукцию тормозных сигналов, адресованных вентро-латеральным центрам голода.
Существует типичный механизм обратной связи между уровнем лептина и выработкой гипоталамического нейропептида Y. Нейропептид Y стимулирует пищевое поведение, потребление пищи, продукцию инсулина и, наконец, накопление жира в адипоцитах. Все периферические и центральные влияния, снижающие аппетит, например, холицистокининовые, проявляются через снижение продукции нейропептида Y.
В этих условиях энергетические траты организма снижаются до минимума, а процессы липогенеза значительно преобладают над липолитическими. Более того, лептин — стимулятор центров теплопродукции, активатор норадренергических симпатических механизмов, обеспечивающих после достижения сытости увеличение калорических затрат. Он способствует увеличению термогенеза, поскольку активирует норадренергический липолиз в жировой ткани через адренорецепторы.
Открытие этого гормона заставило ученых изменить взгляд на ожирение. Уже стало привычным называть лептин «голосом жировой ткани». Таким образом, у подавляющего большинства тучных людей уровень лептина повышен.
На сегодняшний день уже сформулировано понятие лептинорезистентности — это резистентность к лептину, которая может сочетаться с инсулинорезистентностью.
Причины развития лептинорезистентности и возможности ее коррекции, а также реальные пути влияния на состояние ожирения при помощи лептина или его аналогов изучены недостаточно.
Синдром ожирения следует рассматривать как состояние общей метаболической резистентности к липолитическим влияниям. Формирующаяся при этом нечувствительность тканей к лептину и, особенно, к инсулину приводит к патологически высокой активации процессов липосинтеза за счет реактивной гиперинсулинемии.
Изучение лептиновой регуляции у лиц с первичным ожирением показало, что около 20% подобных тучных больных имеют абсолютную лептиновую недостаточность.
У более 80% пациентов, страдающих первичным ожирением, выражена гиперлептинемия. Таким образом, у них можно предполагать наличие первичной лептинорезистентности или относительной недостаточности действия лептина на гипоталамус. Во втором случае, несмотря на наличие лептина, центр голода продолжает активную выработку нейропептида Y.
С другой стороны, даже кратковременные ограничения в приеме пищи, приводящие к незначительной потере жировой массы и, соответственно, к снижению концентрации инсулина и лептина, вызывают реакцию гипоталамических центров регуляции, направленную на сохранение имеющихся жировых ресурсов.
При этом формируется порочный круг, составляющий основу любого вида ожирения. Все большая доля потребляемых пищевых веществ, чрезмерная и не уравновешенная противоположными влияниями процессов липосинтеза, трансформируется в метаболически инертную жировую массу таким образом, что организм, чтобы обеспечить непомерно возрастающие при ожирении метаболические потребности, вынужден поглощать все большее количество пищи.
Кроме того, снижение двигательной активности приводит к формированию инсулинрезистентности мышечной, а затем и других тканей, вследствие чего эффективность усвоения и утилизации глюкозы клетками организма резко снижена, несмотря на патологически высокие уровни гликемии.
Складывается парадоксальная ситуация: организм, обладающий огромными запасами энергии в виде жировой ткани, не способен их адекватно расходовать, несмотря на переедание, и находится в состоянии клеточного голодания.
Более того, в организме больного ожирением очень скоро формируется характерный метаболический синдром, составляющими которого являются гиперинсулинемия, инсулинорезистентность периферических тканей, гипергликемия, гиперлипидемия и гиперхолестеринемия.
Таблица 3. Тактика лечения больных с МС без АГ
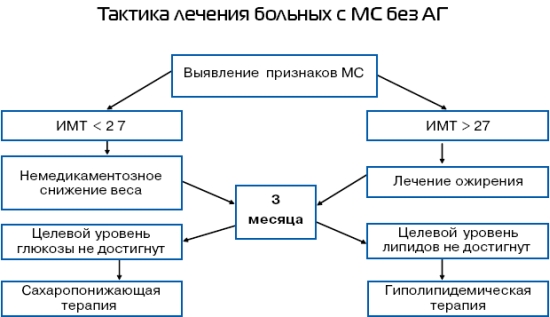
Выделение МС имеет большое клиническое значение, поскольку это состояние является обратимым: при соответствующем своевременном лечении можно добиться исчезновения или, по крайней мере, уменьшения выраженности основных его проявлений и серьезнейших осложнений.
